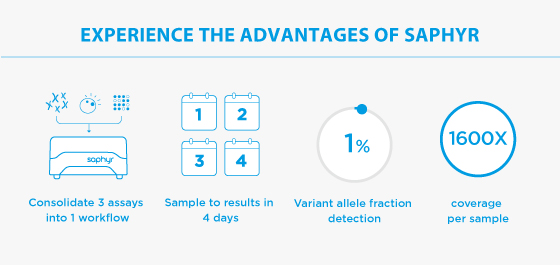
재배열, 누락 또는 부러지거나 잉여 염색체를 감지하면 질병을 진단하고 치료 옵션을 찾을 수 있지만, 전통적인 세포유전학적 방법은 해상도 및 속도면에서 제한적입니다. Saphyr는 모든 CNV, 염색체 이상 및 구조적 변이를 감지하고 기존의 세포유전학적 분석을 하나의 단일 워크플로로 통합할 수 있습니다.

임상 샘플에서 구조 변이가 감지되는 방법은 지난 수십 년 동안 최소한으로 발전해 왔으며, 주로 karyotyping, fluorescent in situ Hybridization (FISH) 그리고 array를 기반한 기술과 같이 전통적인 세포유전학적 기술에 의존하고 있습니다. 그러나 이들은 복잡한 실험에서 활용되기에는 기술적 한계가 있으며, 환자 또는 종양 genome에 대한 완전한 치료 및 예후 진단을 제공하기 위해서는 MLPA, qPCR, RNAseq와 같은 분자 기술과의 결합 및 보완이 필요합니다.
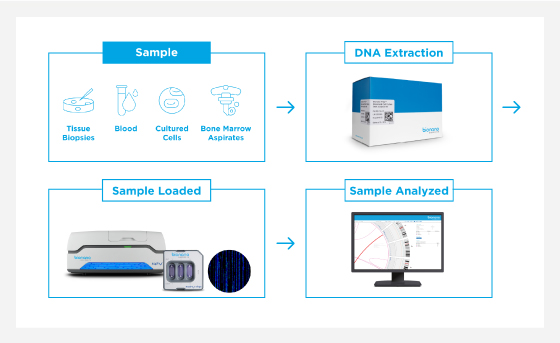
Bionano Genome Imaging은 karyotyping이 수행되는 방식과 유사하게 유전체를 시각화합니다. 이것은 intact DNA에 marker banding 패턴을 직접적으로 시각화하는 것입니다. 이러한 band들 50만개를 게놈에 적용하였고, 메가베이스 크기의 분자를 linearize하는 nanochannel array에서 매우 높은 처리량과 자동화된 방식으로 imaging이 수행됩니다. 이는 karyotyping보다 10,000x 더 높은 해상도로 event를 연구할 수 있게 합니다. 500bp에서 insertion 및 deletion, vs 염색체 banding 분석을 통해 ~5Mbp 를 볼 수 있습니다. 시료 당 수집된 1600x의 게놈 커버리지로 1% variant allele fraction (VAF)까지 구조 변이를 찾을 수 있습니다.

BIONANO는 모든 유형의 구조 변이를
매우 민감하게 감지합니다.
현재까지 Bionano는 karyotyping, FISH 그리고 microarray를 통합하여 검출된
모든 임상적으로 보고된 변이들을 100% 전부 발견했으며,
특히 누락된 부분들을 많이 찾아내었습니다.
A large collaborative, multi-center study led by Columbia University
컬럼비아 대학이 주도한 대규모의 협력적 멀티센터 연구는 Bionano를 혈종양 치료의 기준과 비교합니다: 2020년 5월에 암 유전체학 컨소시엄 (Cancer Genomics Consortium) 웨비나에서 제시된 예비 결과는 분석된 91개 모든 샘플에 적용된 karyotyping과 100% 일치하고, 이 실험이 적용된 sample들의 subset에 적용된 array와 FISH와도 일치함을 보여주었습니다. |
A study by MD Anderson Cancer Center
MD Anderson Cancer Center의 연구는 MDS(Myelodysplastic Syndrome) 환자에 적용된 Bionano 기술과 기존의 cytogenetic 방법을 비교해 보았습니다. 13개의 MDS 샘플에 대한 결과는 karyotype 및 array에 비해 10% 이상의 allele fration에서 변이를 100% 감지하는 데 성공했으며, 세포유전학 방법에서 누락된 많은 변이들과 복잡한 구간들이 발견되었습니다. |
Identification of Hidden Structural Variations
With Optical Genome Mapping - Bionano Genomics
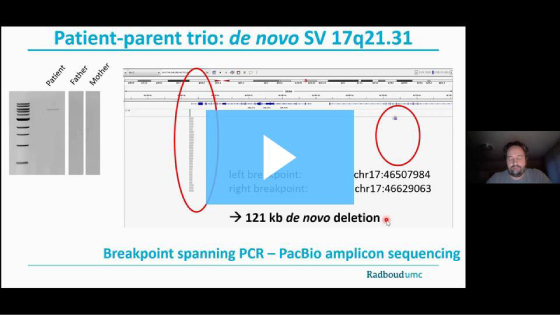
네덜란드의 Radboud University Medical Center(RUMC)의 Alexander Hoischen 박사가 이끄는 또 다른 팀은 백혈병 genome의 임상 분석을 위한 Bionano Genomics의 Saphyr® 시스템 검증은 성공적이었다고 보고했습니다. bioRxiv에서 발표된 연구는 Saphyr가 체세포 염색체의 이상 감지 기준과 100% 일치한다는 것을 알아냈습니다. RUMC 클리닉의 가장 흔한 사례인 골수성(myeloid) 및 림프성 (lymphoid) 백혈병이 결합된 총 48개의 환자 샘플들을 standard cytogenetic 분석법을 통해 연구했습니다. 모든 샘플은 최소 10%의 병원성 변이의 allele fraction을 가지고 있었습니다. 큰 구조적 이상(structural abnormality)의 수에 따라 37개의 샘플은 simple, 11개의 샘플은 complex 카테고리로 분류되었습니다. 이후 Bionano를 활용하여 48개의 모든 샘플을 분석했을 때, 연구진은 이전에 보고되었던 모든 이상을 확인할 수 있었습니다. 또한 Bionano는 더 나은 해상도를 제공하고 복잡한 이상현상을 더 완벽하게 보여줄 수 있었습니다. 복잡한 chromothripsis 구조가 뚜렷하게 분석되었고, 다른 경우에는 additional fusion이 확인되거나 origin을 알 수 없는 marker 염색체가 분석되었습니다. 다른 몇 가지 연구들이 현재 진행 중이며, 지금까지 모두 유사한 예비 결과가 나왔습니다.
“ Whole-genome optical mapping을 활용한 골수종 세포(myeloma cell) 연구를 통해 골수 외 다발성 골수종(extramedullary multiple myeloma; EMM)과 1번 염색체 이상과의 연관성을 밝혀내다 ”

Kriegova et al. (2021)
DOI: 10.1038/s41598-021-93835-z
다발성 골수종 (Multiple Myeloma; MM)은 단일 클론에서 유래하는 형질세포의 악성증식성질환으로, 일반적으로는 골수(bone marrow; BM) 미세 환경에 국한되어 있습니다. MM 환자들은 드물게 골수외 다발성 골수종(extramedullary multiple myeloma; EMM)을 가지고 있으며 이로 인해 골수종 세포가 다른 장기들로 전이됩니다. EMM은 고위험 cytogenetics와 깊은 관련이 있지만, 그들의 복잡한 유전적 구조에 대한 정보는 현재 부족한 상황입니다.
본 연구에서는 최신 기술인 whole-genome optical mapping (Saphyr, Bionano Genomics)이 MM과 EMM 환자의 BM 골수종 세포의 유전체 구조를 분석하기 위해 활용되었습니다. 이 기술은 크고 작은 구조적 재배열 뿐만 아니라 NGS 및 cytogenetics와 같은 기존의 방법으로는 감지할 수 없었던 게놈 전체에 걸친 복잡한 재배열도 분석할 수 있다는 장점이 있습니다.
EMM에서의 유전적 구조를 분석하여 그 특징을 알아내는 것은 EMM 발병에 대한 이해를 돕고 새로운 예후 및 진단을 위한 바이오마커를 찾아내는데 크게 기여할 것입니다.